Uptravi
filmovertrukne tabletter 200 mikrogram, 400 mikrogram, 600 mikrogram, 800 mikrogram, 1000 mikrogram, 1200 mikrogram, 1400 mikrogram og 1600 mikrogram
Janssen
Om indlægssedlen
Indlægsseddel: Information til patienten
Uptravi 100 mikrogram filmovertrukne tabletter
Uptravi 200 mikrogram filmovertrukne tabletter
Uptravi 400 mikrogram filmovertrukne tabletter
Uptravi 600 mikrogram filmovertrukne tabletter
Uptravi 800 mikrogram filmovertrukne tabletter
Uptravi 1 000 mikrogram filmovertrukne tabletter
Uptravi 1 200 mikrogram filmovertrukne tabletter
Uptravi 1 400 mikrogram filmovertrukne tabletter
Uptravi 1 600 mikrogram filmovertrukne tabletter
Selexipag
Læs denne indlægsseddel grundigt, inden du begynder at tage dette lægemiddel, da den indeholder vigtige oplysninger.
- Gem indlægssedlen. Du kan få brug for at læse den igen.
- Spørg lægen eller sygeplejersken, hvis der er mere, du vil vide.
- Lægen har ordineret dette lægemiddel til dig personligt. Lad derfor være med at give lægemidlet til andre. Det kan være skadeligt for andre, selvom de har de samme symptomer, som du har.
- Kontakt lægen eller sygeplejersken, hvis du får bivirkninger, herunder bivirkninger, som ikke er nævnt i denne indlægsseddel. Se afsnit 4.
Se den nyeste indlægsseddel på www.indlaegsseddel.dk
Oversigt over indlægssedlen:
- Virkning og anvendelse
- Det skal du vide, før du begynder at tage Uptravi
- Sådan skal du tage Uptravi
- Bivirkninger
- Opbevaring
- Pakningsstørrelser og yderligere oplysninger
1. Virkning og anvendelse
Uptravi er et lægemiddel, der indeholder det aktive stof selexipag. Det har samme afslappende og udvidende virkning på blodkarrene som det naturlige stof prostacyklin.
Uptravi anvendes til langvarig behandling af pulmonal arteriel hyptertension (PAH) hos voksne patienter, som ikke kan opnå tilstrækkelig effekt med andre typer af lægemidler mod PAH, der kaldes for endothelinreceptorantagonister og phosphodiesterase type 5-hæmmere. Uptravi kan anvendes alene, hvis patienten ikke er kandidat til disse lægemidler.
PAH er højt blodtryk i de blodkar, der fører blod fra hjertet til lungerne (lungearterierne). Hos personer, der har PAH, bliver disse arterier smallere, så hjertet skal arbejde hårdere for at pumpe blod igennem dem. Dette kan forårsage træthed, svimmelhed, stakåndethed eller andre symptomer.
Dette lægemiddel virker på samme måde som det naturlige stof prostacyklin, så det udvider lungearterierne og gør dem mindre hårde. Dermed bliver det nemmere for hjertet at pumpe blod igennem lungearterierne. Uptravi sænker trykket i lungearterierne, lindrer symptomerne på PAH og gør, at PAH-sygdommen udvikler sig langsommere.
2. Det skal du vide, før du begynder at tage Uptravi
Tag ikke Uptravi
- hvis du er allergisk over for selexipag eller et af de øvrige indholdsstoffer i Uptravi (angivet i afsnit 6).
- hvis du har et hjerteproblem, såsom:
- dårlig blodforsyning til hjertemusklerne (alvorlig koronarhjertesygdom eller ustabil angina); symptomerne kan omfatte brystsmerter
- hjerteanfald inden for de sidste 6 måneder
- svagt hjerte (dekompenseret hjertesvigt), som ikke er under tæt lægeligt opsyn
- alvorligt uregelmæssigt hjerteslag
- hjerteklapfejl (medfødt eller erhvervet), der medfører, at hjertet arbejder dårligt (ikke relateret til pulmonal hypertension)
- hvis du har haft et slagtilfælde inden for de seneste 3 måneder, eller der er forekommet andre hændelser, der har mindsket blodforsyningen til hjernen (f.eks. transitorisk cerebral iskæmi)
- hvis du tager gemfibrozil (lægemiddel, der anvendes til at sænke niveauet af fedt [lipider] i blodet).
Advarsler og forsigtighedsregler
Kontakt PAH-lægen eller sygeplejersken, før du tager Uptravi, hvis du
- tager medicin mod højt blodtryk
- har lavt blodtryk, der er forbundet med symptomer såsom svimmelhed
- for nylig har mistet meget blod eller væske, f.eks. som følge af alvorlig diarré eller opkastning
- har problemer med skjoldbruskkirtlen
- har alvorlige nyreproblemer eller er i dialyse
- har eller har haft alvorlige leverfunktionsproblemer
Fortæl det straks til lægen, hvis du bemærker et af ovenstående tegn, eller din tilstand forandres.
Børn og unge
Giv ikke dette lægemiddel til børn under 18 år.
Ældre patienter
Der er begrænset erfaring med Uptravi hos patienter over 75 år. Uptravi skal anvendes med forsigtighed i denne aldersgruppe.
Brug af andre lægemidler sammen med Uptravi
Fortæl det altid til lægen, hvis du tager andre lægemidler, for nylig har taget andre lægemidler eller planlægger at tage andre lægemidler.
Brug af andre lægemidler kan påvirke Uptravis virkning.
Fortæl det til PAH-lægen eller sundhedspersonalet, hvis du tager et eller flere af følgende lægemidler:
- Gemfibrozil (lægemiddel, der anvendes til at sænke niveauet af fedt [lipider] i blodet)
- Clopidogrel (lægemiddel, der anvendes til at hæmme dannelsen af blodpropper ved koronararteriesygdom)
- Deferasirox (lægemiddel, der anvendes til at fjerne jern fra blodet)
- Teriflunomid (lægemiddel, der anvendes til behandling af recidiverende-remitterende multipel sklerose)
- Carbamazepin (lægemiddel, der anvendes til behandling af visse former for epilepsi, nervesmerter eller som hjælp til at kontrollere alvorlige humørsvingninger, når andre lægemidler ikke virker)
- Phenytoin (lægemiddel, der anvendes til behandling af epilepsi)
- Valproinsyre (lægemiddel, der anvendes til behandling af epilepsi)
- Probenecid (lægemiddel, der anvendes til behandling af urinsyregigt)
- Fluconazol, rifampicin eller rifapentin (antibiotika, der anvendes til behandling af infektioner).
Graviditet og amning
Uptravi frarådes under graviditet og amning. Hvis du er en kvinde i den fødedygtige alder, skal du anvende sikker prævention, mens du tager Uptravi. Hvis du er gravid eller ammer, har mistanke om, at du er gravid, eller planlægger at blive gravid, skal du spørge lægen til råds, før du tager dette lægemiddel.
Trafik- og arbejdssikkerhed
Uptravi kan forårsage bivirkninger, såsom hovedpine og lavt blodtryk (se afsnit 4), der kan påvirke din evne til at føre motorkøretøj; symptomerne ved din sygdom kan også nedsætte din evne til at føre motorkøretøj.
3. Sådan skal du tage Uptravi
Uptravi må kun ordineres af en læge med erfaring i behandling af PAH. Tag altid lægemidlet nøjagtigt efter lægens anvisning. Er du i tvivl eller har spørgsmål, så spørg lægen.
Fortæl det til lægen, hvis du oplever bivirkninger, da lægen kan anbefale, at du ændrer din dosis af Uptravi.
Fortæl det til lægen, hvis du har problemer med leveren eller tager andre lægemidler, da lægen kan anbefale, at du tager en lavere dosis af Uptravi to gange dagligt eller kun tager det én gang dagligt.
Hvis dit syn er nedsat, eller du har en form for blindhed, skal du have hjælp fra en anden person, når du tager Uptravi i titreringsperioden (perioden hvor din dosis gradvist forøges).
Sådan findes der frem til den rette dosis for dig
Hvis lægen ordinerer 200 mikrogram-tabletter
I starten af behandlingen vil de fleste patienter tage en 200 mikrogram-tablet om morgenen og endnu én 200 mikrogram-tablet om aftenen, med ca. 12 timers mellemrum. Det anbefales at starte behandlingen om aftenen. Lægen vil anvise, at du gradvist øger dosis. Dette kaldes for titrering. Det giver kroppen mulighed for at vænne sig til den nye medicin. Formålet med titrering er at nå den mest velegnede dosis. Det vil være den højeste dosis, som du kan tolerere, dog højst 1 600 mikrogram om morgenen og om aftenen.
Den første tabletpakning, du får, indeholder lysegule 200 mikrogram-tabletter.
Lægen vil anvise, at du øger din dosis i trin, som regel hver uge, men intervallet mellem stigningerne kan være længere.
Ved hvert trin føjer du en 200 mikrogram-tablet til din morgendosis og en 200 mikrogram-tablet til din aftendosis. Det anbefales, at du tager den første øgede dosis om aftenen. Diagrammet nedenfor viser antallet af tabletter, der skal tages hver morgen og hver aften i de første 4 trin.
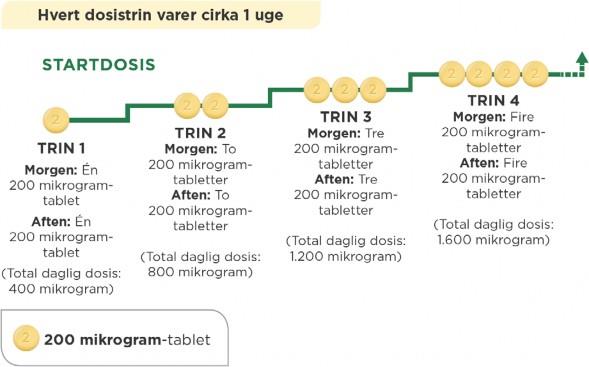
Hvis lægen fortæller dig, at du skal øge din dosis yderligere, skal du føje en 200 mikrogram-tablet til din morgendosis og en 200 mikrogram-tablet til din aftendosis ved hvert nye trin. Det anbefales, at du tager den første øgede dosis om aftenen.
Hvis lægen anviser, at du skal øge din dosis yderligere og gå til trin 5, kan du gøre det ved at tage én grøn 800 mg-tablet og én lysegul 200 mikrogram-tablet om morgenen og én 800 mikrogram-tablet og én 200 mikrogram-tablet om aftenen.
Den højeste dosis af Uptravi er 1 600 mikrogram om morgenen og 1 600 mikrogram om aftenen. Det er dog ikke alle patienter, der når denne dosis, da den påkrævede dosis varierer fra patient til patient.
Diagrammet nedenfor viser hvor mange tabletter, der skal tages hver morgen og hver aften på hvert trin fra og med trin 5.
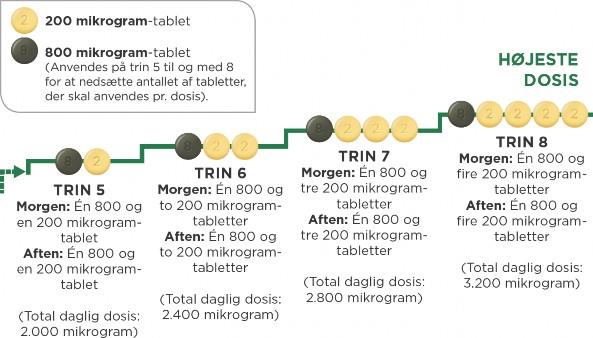
Hvis lægen ordinerer 100 mikrogram-tabletter
Hvis du har problemer med leveren eller tager visse andre lægemidler, kan lægen ordinere 100 mikrogram-tabletter som din startdosis.
I starten af behandlingen skal du tage én 100 mikrogram-tablet om morgenen og endnu én 100 mikrogram-tablet om aftenen, med ca. 12 timers mellemrum. Det anbefales at starte behandlingen om aftenen. Lægen vil anvise, at du gradvist øger dosis. Dette kaldes for titrering. Det giver kroppen mulighed for at vænne sig til det nye lægemiddel. Formålet med titrering er at nå den mest velegnede dosis. Det vil være den højeste dosis, som du kan tåle, dog højst 800 mikrogram om morgenen og om aftenen.
Lægen vil anvise, at du skal øge din dosis i trin, som regel hver uge, men intervallet mellem dosisøgningerne kan være længere.
Ved hvert trin føjer du en 100 mikrogram-tablet til din morgendosis og en anden 100 mikrogramtablet til din aftendosis. Det anbefales, at du tager den første øgede dosis om aftenen. Se titreringsvejledningen til patienter, der er vedlagt i titreringspakken, for at få oplysninger om, hvordan du optrapper din dosis.
Fortæl det til lægen, hvis du holder op med eller overvejer at holde op med at tage andre lægemidler, da det kan være nødvendigt at justere din dosis af selexipag.
Hvis lægen fortæller dig, at du skal øge din dosis yderligere, skal du føje en 100 mikrogram-tablet til din morgendosis og en 100 mikrogram-tablet til din aftendosis ved hvert nyt trin. Det anbefales, at du tager den første øgede dosis om aftenen.
Hvis lægen anviser, at du skal øge din dosis til over 400 mikrogram, kan du gøre det ved at tage én rød 400 mg-tablet og én lysegul 100 mikrogram-tablet om morgenen og én 400 mikrogram-tablet og én 100 mikrogram-tablet om aftenen. Se titreringsvejledningen til patienter, der er vedlagt i titreringspakken, for at få oplysninger om, hvordan du optrapper din dosis.
Ved optitrering med 100 mikrogram-tabletterne er den højeste dosis af Uptravi 800 mikrogram om morgenen og 800 mikrogram om aftenen. Det er dog ikke alle patienter, der når denne dosis, da den nødvendige dosis varierer fra patient til patient.
Brug af titreringsvejledningen under titrering
Du får en titreringspakke, som indeholder en titreringsvejledning og en indlægsseddel.
Titreringsvejledningen indeholder oplysninger om titreringsforløbet, og du kan notere i den, hvor mange tabletter du tager hver dag.
Husk at notere i din titreringsdagbog, hvor mange tabletter du tager hver dag. Titreringstrinene varer som regel omkring 1 uge. Hvis lægen anviser, at hvert titreringstrin skal vare længere end 1 uge, er der flere dagbogssider, hvor du kan notere dette. Husk, at du skal være i regelmæssig kontakt med PAH-lægen eller sundhedspersonalet i titreringsforløbet.
Nedtrapning til en lavere dosis på grund af bivirkninger
I titreringsforløbet kan du få bivirkninger, såsom hovedpine, diarré, kvalme, opkastning, smerter i kæben, muskelsmerter, smerter i benene, ledsmerter eller ansigtsrødme (se afsnit 4). Hvis du har svært ved at tolerere disse bivirkninger, så drøft med lægen, hvordan de kan håndteres eller behandles. Der findes behandlinger, der kan bidrage til at lindre bivirkningerne. For eksempel kan smertestillende midler såsom paracetamol være en hjælp til behandling af smerter og hovedpine.
Hvis bivirkningerne ikke kan behandles eller ikke bliver gradvist bedre med den dosis, du tager, vil lægen eventuelt justere din dosis ved at nedsætte antallet af lysegule tabletter med én om morgenen og én om aftenen. Diagrammet nedenfor viser nedtrapning til en lavere dosis. Gør kun dette, hvis lægen har anvist det.
Titrering med 200 mikrogram-tabletter
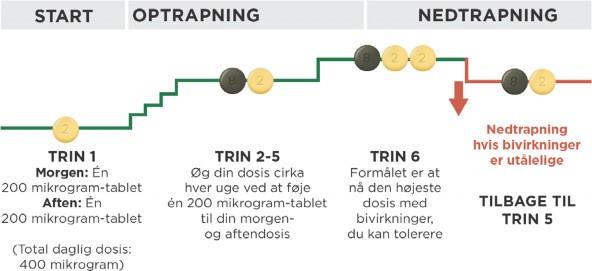
Hvis du titrerer med 100 mikrogram-tabletter, kan du finde oplysninger om, hvordan du nedtrapper, i titreringsvejledningen til patienter, der er vedlagt i titreringspakken.
Hvis dine bivirkninger bliver tålelige efter nedtrapning af din dosis, vil lægen eventuelt beslutte, at du skal fortsætte med den dosis. Se venligst afsnittet ’Vedligeholdelsesdosis’ nedenfor for yderligere oplysninger.
Vedligeholdelsesdosis
Den højeste dosis, som du kan tolerere i titreringsfasen, vil blive din vedligeholdelsesdosis. Din vedligeholdelsesdosis er den dosis, som du skal fortsætte med at tage regelmæssigt.
Lægen vil ordinere en eller flere tabletter med den eller de for dig individuelt tilpassede styrker, som vil være din vedligeholdelsesdosis. På denne måde kan du måske nøjes med at tage én tablet om morgenen og én om aftenen, i stedet for flere tabletter hver gang.
Du finder en fuld beskrivelse af Uptravi tabletter, herunder farver og mærkning, i afsnit 6.
Med tiden vil lægen eventuelt justere din vedligeholdelsesdosis efter behov.
Hvis du på et tidspunkt efter at have taget den samme dosis i lang tid får bivirkninger, som du ikke kan tolerere, eller bivirkninger, der påvirker dine dagligdagsaktiviteter, skal du kontakte lægen, da det kan være, at din dosis skal nedsættes. Lægen vil eventuelt ordinere en lavere dosis. Husk at bortskaffe ikke anvendte tabletter (se afsnit 5).
Tag Uptravi én gang om morgenen og én gang om aftenen med cirka 12 timers mellemrum.
Tag tabletterne i forbindelse med måltider, da det kan medvirke til, at du bedre kan tåle lægemidlet. Tabletovertrækket er en beskyttelse. Tabletterne skal synkes hele med et glas vand. Tabletterne må ikke deles eller knuses.
Hvis du har taget for meget Uptravi
Spørg lægen til råds, hvis du har taget flere tabletter, end lægen har anvist.
Hvis du har glemt at tage Uptravi
Hvis du glemmer at tage Uptravi, skal du tage en dosis, så snart du kommer i tanker om det. Herefter skal du fortsætte med at tage tabletterne på det sædvanlige tidspunkt. Hvis det næsten er tid til næste dosis (under 6 timer til det normale tidspunkt), skal du springe den glemte dosis over og fortsætte med at tage lægemidlet til sædvanlig tid. Du må ikke tage en dobbeltdosis som erstatning for den glemte tablet.
Hvis du holder op med at tage Uptravi
Brat ophør af behandlingen med Uptravi kan resultere i, at dine symptomer bliver forværrede. Du må ikke stoppe med at tage Uptravi, medmindre lægen anviser det. Lægen vil eventuelt anvise, at du nedsætter dosis gradvist, før du stopper helt.
Hvis du af en hvilken som helst årsag stopper med at tage Uptravi i mere end 3 dage i træk (hvis du har glemt 3 morgen- og 3 aftendoser, eller seks doser eller mere i træk), skal du straks kontakte lægen, da det kan være nødvendigt at justere din dosis for at undgå bivirkninger. Lægen kan beslutte, at du skal genstarte behandlingen med en lavere dosis, som øges gradvist til din tidligere vedligeholdelsesdosis.
Spørg lægen eller sygeplejersken, hvis der er noget, du er i tvivl om.
4. Bivirkninger
Dette lægemiddel kan som alle andre lægemidler give bivirkninger, men ikke alle får bivirkninger. Du kan få bivirkninger, ikke alene i titreringsperioden hvor dosis øges, men også senere efter lang tids brug af samme dosis.
Hvis du oplever hævelse i ansigt, læber, mund, tunge eller svælg, som gør det svært at synke eller trække vejret (angioødem), skal du straks kontakte lægen.
Hvis du får en eller flere af følgende bivirkninger: hovedpine, diarré, kvalme, opkastning, smerter i kæben, muskelsmerter, smerter i benene, ledsmerter eller ansigtsrødme, som du ikke kan tolerere, eller som ikke kan behandles, skal du kontakte lægen, da din dosis kan være for høj og skal nedsættes.
Meget almindelige bivirkninger (kan forekomme hos flere end 1 ud af 10 personer)
- Hovedpine
- Blussen (ansigtsrødme)
- Kvalme og opkastning
- Diarré
- Smerter i kæben, muskelsmerter, ledsmerter, smerter i benene
- Nasofaryngitis (tilstoppet næse)
Almindelige bivirkninger (kan forekomme hos op til 1 ud af 10 personer)
- Anæmi (lavt antal røde blodlegemer)
- Hyperthyreoidisme (overaktiv skjoldbruskkirtel)
- Nedsat appetit
- Vægttab
- Hypotension (lavt blodtryk)
- Mavesmerter, herunder fordøjelsesbesvær
- Smerter
- Ændringer i visse blodprøveresultater, herunder blodprøver til kontrol af blodtal og skjoldbruskkirtlens funktion
- Udslæt, herunder nældefeber, kan forårsage brænden eller svien og hudrødme
- Angioødem og dets symptomer som beskrevet i begyndelsen af dette afsnit
Ikke almindelige bivirkninger (kan forekomme hos op til 1 ud af 100 personer)
- Hurtigere puls
Indberetning af bivirkninger
Hvis du oplever bivirkninger, bør du tale med lægen. Dette gælder også mulige bivirkninger, som ikke er medtaget i denne indlægsseddel. Du eller dine pårørende kan også indberette bivirkninger direkte til Lægemiddelstyrelsen via de oplysninger, der fremgår herunder.
Lægemiddelstyrelsen
Axel Heides Gade 1
DK-2300 København S
Websted: www.meldenbivirkning.dk
Ved at indrapportere bivirkninger kan du hjælpe med at fremskaffe mere information om sikkerheden af dette lægemiddel.
5. Opbevaring
Opbevar lægemidlet utilgængeligt for børn.
Brug ikke Uptravi efter den udløbsdato, der står på æsken og på blisteren eller beholderens etiket efter EXP. Udløbsdatoen er den sidste dag i den nævnte måned.
Brug Uptravi 100 mikrogram filmovertrukne tabletter inden 3 måneder efter første åbning eller inden udløbsdatoen (hvad end der forekommer først).
Dette lægemiddel kræver ingen særlige forholdsregler vedrørende opbevaringen.
Spørg apotekspersonalet, hvordan du skal bortskaffe lægemiddelrester. Af hensyn til miljøet må du ikke smide lægemiddelrester i afløbet, toilettet eller skraldespanden.
6. Pakningsstørrelser og yderligere oplysninger
Uptravi indeholder:
Aktivt stof: selexipag.
Uptravi 100 mikrogram filmovertrukne tabletter indeholder 100 mikrogram selexipag
Uptravi 200 mikrogram filmovertrukne tabletter indeholder 200 mikrogram selexipag
Uptravi 400 mikrogram filmovertrukne tabletter indeholder 400 mikrogram selexipag
Uptravi 600 mikrogram filmovertrukne tabletter indeholder 600 mikrogram selexipag
Uptravi 800 mikrogram filmovertrukne tabletter indeholder 800 mikrogram selexipag
Uptravi 1 000 mikrogram filmovertrukne tabletter indeholder 1 000 mikrogram selexipag
Uptravi 1 200 mikrogram filmovertrukne tabletter indeholder 1 200 mikrogram selexipag
Uptravi 1 400 mikrogram filmovertrukne tabletter indeholder 1 400 mikrogram selexipag
Uptravi 1 600 mikrogram filmovertrukne tabletter indeholder 1 600 mikrogram selexipag
Øvrige indholdsstoffer:
Tabletkerne
Mannitol (E421)
Majsstivelse
Lavsubstitueret hydroxypropylcellulose
Hydroxypropylcellulose
Magnesiumstearat
Filmovertræk
Hypromellose (E464)
Propylenglycol (E1520)
Titandioxid (E171)
Jernoxider (E172)
Carnaubavoks
Uptravi 100 mikrogram filmovertrukne tabletter indeholder gul jernoxid, sort jernoxid (E172) og talcum.
Uptravi 200 mikrogram filmovertrukne tabletter indeholder gul jernoxid (E172).
Uptravi 400 mikrogram filmovertrukne tabletter indeholder rød jernoxid (E172).
Uptravi 600 mikrogram filmovertrukne tabletter indeholder rød jernoxid og sort jernoxid (E172).
Uptravi 800 mikrogram filmovertrukne tabletter indeholder gul jernoxid og sort jernoxid (E172).
Uptravi 1 000 mikrogram filmovertrukne tabletter indeholder rød jernoxid og gul jernoxid (E172).
Uptravi 1 200 mikrogram filmovertrukne tabletter indeholder sort jernoxid og rød jernoxid (E172).
Uptravi 1 400 mikrogram filmovertrukne tabletter indeholder gul jernoxid (E172).
Uptravi 1 600 mikrogram filmovertrukne tabletter indeholder sort jernoxid, rød jernoxid og gul jernoxid (E172).
Udseende og pakningsstørrelser
Uptravi 100 mikrogram filmovertrukne tabletter: Runde, lysegule, filmovertrukne tabletter med en diameter på 3,0 mm, der er mærket med "1" på den ene side.
Uptravi 200 mikrogram filmovertrukne tabletter: Runde, lysegule, filmovertrukne tabletter med en diameter på 7,3 mm, der er mærket med "2" på den ene side.
Uptravi 400 mikrogram filmovertrukne tabletter: Runde, røde, filmovertrukne tabletter med en diameter på 7,3 mm, der er mærket med "4" på den ene side.
Uptravi 600 mikrogram filmovertrukne tabletter: Runde, lyslilla, filmovertrukne tabletter med en diameter på 7,3 mm, der er mærket med "6" på den ene side.
Uptravi 800 mikrogram filmovertrukne tabletter: Runde, grønne, filmovertrukne tabletter med en diameter på 7,3 mm, der er mærket med "8" på den ene side.
Uptravi 1 000 mikrogram filmovertrukne tabletter: Runde, orange, filmovertrukne tabletter med en diameter på 7,3 mm, der er mærket med "10" på den ene side.
Uptravi 1 200 mikrogram filmovertrukne tabletter: Runde, mørkelilla, filmovertrukne tabletter med en diameter på 7,3 mm, der er mærket med "12" på den ene side.
Uptravi 1 400 mikrogram filmovertrukne tabletter: Runde, mørkegule, filmovertrukne tabletter med en diameter på 7,3 mm, der er mærket med "14" på den ene side.
Uptravi 1 600 mikrogram filmovertrukne tabletter: Runde, brune, filmovertrukne tabletter med en diameter på 7,3 mm, der er mærket med "16" på den ene side.
Uptravi 100 mikrogram filmovertrukne tabletter leveres i beholdere med 60 og 140 tabletter (titreringspakker).
Uptravi 200 mikrogram filmovertrukne tabletter leveres i blisterpakninger med 10 eller 60 tabletter og 60 eller 140 tabletter (titreringspakker).
Uptravi 400 mikrogram, 600 mikrogram, 800 mikrogram, 1 000 mikrogram, 1 200 mikrogram, 1 400 mikrogram og 1 600 mikrogram filmovertrukne tabletter leveres i blisterpakninger med 60 tabletter.
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
Indehaver af markedsføringstilladelsen og fremstiller
Indehaver af markedsføringstilladelsen
Janssen-Cilag International NV
Turnhoutseweg 30
B-2340 Beerse
Belgien
Fremstiller
Janssen Pharmaceutica NV
Turnhoutseweg 30
B-2340 Beerse
Belgien
Hvis du ønsker yderligere oplysninger om dette lægemiddel, skal du henvende dig til den lokale repræsentant for indehaveren af markedsføringstilladelsen:
Danmark
Janssen-Cilag A/S
Tlf.: +45 4594 8282
jacdk@its.jnj.com
Du kan finde yderligere oplysninger om dette lægemiddel på Det Europæiske Lægemiddelagenturs hjemmeside https://www.ema.europa.eu.
Revisionsdato
Denne indlægsseddel blev senest ændret 12/2024.


