IMULDOSA®
injektionsvæske, opløsning i fyldt injektionssprøjte 45 mg
Accord
Om indlægssedlen
Indlægsseddel: Information til brugeren
IMULDOSA 45 mg injektionsvæske, opløsning
ustekinumab
▼Dette lægemiddel er underlagt supplerende overvågning. Dermed kan der hurtigt tilvejebringes nye oplysninger om sikkerheden. Du kan hjælpe ved at indberette alle de bivirkninger, du får. Se sidst i punkt 4, hvordan du indberetter bivirkninger.
Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger.
Denne indlægsseddel er skrevet til den person, der tager lægemidlet. Forældre eller omsorgspersoner, som skal give IMULDOSA til et barn, skal læse indlægssedlen grundigt.
- Gem indlægssedlen. Du kan få brug for at læse den igen.
- Spørg lægen eller apotekspersonalet, hvis der er mere, du vil vide.
- Lægen har ordineret dette lægemiddel til dig personligt. Lad derfor være med at give lægemidlet til andre. Det kan være skadeligt for andre, selvom de har de samme symptomer, som du har.
- Kontakt lægen eller apotekspersonalet, hvis du får bivirkninger, herunder bivirkninger, som ikke er nævnt i denne indlægsseddel. Se punkt 4.
Se den nyeste indlægsseddel på www.indlaegsseddel.dk.
Oversigt over indlægssedlen:
- Virkning og anvendelse
- Det skal du vide, før du begynder at bruge IMULDOSA
- Sådan skal du bruge IMULDOSA
- Bivirkninger
- Opbevaring
- Pakningsstørrelser og yderligere oplysninger
1. Virkning og anvendelse
Virkning
IMULDOSA indeholder det aktive stof ustekinumab, et antistof, der er fremstillet ud fra en enkelt klonet celle (monoklonalt). Monoklonale antistoffer er proteiner, som genkender og bindes specifikt til visse proteiner i kroppen.
IMULDOSA tilhører en gruppe lægemidler, der kaldes immunsuppressiva (immundæmpende lægemidler). Disse lægemidler virker ved at svække dele af immunsystemet.
Anvendelse
IMULDOSA bruges til at behandle følgende betændelseslignende tilstande:
- Plaque-psoriasis hos voksne og børn på 6 år og derover
- Psoriasisartrit hos voksne
- Moderat til alvorlig Crohns sygdom hos voksne
Plaque-psoriasis
Plaque-psoriasis er en hudsygdom, der giver en betændelseslignende tilstand (inflammation) i huden og neglene. IMULDOSA mindsker inflammationen og andre tegn på sygdommen.
IMULDOSA bruges til voksne med moderat til alvorlig plaque-psoriasis, der ikke kan bruge ciclosporin, methotrexat eller lysbehandling, eller i tilfælde, hvor disse behandlinger ikke virker.
IMULDOSA bruges til børn og unge på 6 år og derover med moderat til alvorlig plaque-psoriasis, som ikke tåler lysbehandling eller andre systemiske behandlinger, eller hvis disse behandlinger ikke virker.
Psoriasisartrit
Psoriasisartrit er en betændelseslignende tilstand i leddene, der sædvanligvis ledsages af psoriasis. Hvis du har aktiv psoriasisartrit, vil du først få andre lægemidler. Hvis du ikke opnår tilstrækkelig virkning af disse lægemidler, kan du få IMULDOSA:
- for at mindske symptomerne på sygdommen
- for at forbedre din fysiske funktion
- for at forhale ledskader.
Crohns sygdom
Crohns sygdom er en betændelseslignende (inflammatorisk) sygdom i tarmen. Hvis du lider af Crohns sygdom, vil du først få andre lægemidler. Hvis du ikke reagerer godt nok på disse lægemidler, eller hvis du ikke kan tåle dem, kan du få IMULDOSA for at mindske symptomerne på din sygdom.
2. Det skal du vide, før du begynder at bruge IMULDOSA
Brug ikke IMULDOSA
- hvis du er allergisk over for ustekinumab eller et af de øvrige indholdsstoffer i IMULDOSA (angivet i afsnit 6).
- hvis du har en aktiv infektion, som din læge anser for at være betydningsfuld.
Hvis du ikke er sikker på, om noget af ovenstående gælder for dig, så tal med din læge eller apotekspersonalet, før du begynder at bruge IMULDOSA.
Advarsler og forsigtighedsregler
Kontakt lægen eller apotekspersonalet, før du bruger IMULDOSA. Lægen vil tjekke dit helbred før hver behandling. Sørg for at fortælle lægen om enhver sygdom, du måtte have, før hver behandling. Kontakt også lægen, hvis du for nylig har været i nærheden af en person, der kunne have tuberkulose. Lægen vil så undersøge dig og teste dig for tuberkulose, før du får IMULDOSA. Hvis din læge mener, at du har risiko for at få tuberkulose, kan du få et lægemiddel til at behandle det.
Vær opmærksom på alvorlige bivirkninger
IMULDOSA kan give alvorlige bivirkninger, der kan omfatte allergiske reaktioner og infektioner. Vær opmærksom på visse tegn på sygdom, mens du bruger IMULDOSA. Se listen over alle disse bivirkninger under "Alvorlige bivirkninger" i afsnit 4.
Kontakt lægen, før du bruger IMULDOSA:
- Hvis du nogensinde har haft en allergisk reaktion på IMULDOSA. Er du i tvivl, så spørg din læge.
- Hvis du har haft kræft. Immundæmpende lægemidler som IMULDOSA svækker dele af immunsystemet. Dette kan øge risikoen for kræft.
- Hvis du er blevet behandlet for psoriasis med andre biologiske lægemidler (et lægemiddel, der er fremstillet ud fra en biologisk kilde, og som normalt gives som en indsprøjtning) - kan risikoen for kræft være forhøjet.
- Hvis du har eller for nylig har haft en infektion.
- Hvis du har fået nye skader i huden eller forandringer i områder med psoriasis eller på normal hud.
- Hvis du får anden behandling for psoriasis og/eller psoriasisartrit - såsom et andet immundæmpende lægemiddel eller lysbehandling (når kroppen behandles med en type ultraviolet (UV) lys). Disse behandlinger kan også svække dele af immunsystemet. Samtidig brug af disse behandlinger og IMULDOSA er ikke undersøgt. Det er muligt, at det øger risikoen for sygdomme, der forbindes med et svækket immunsystem.
- Hvis du får eller tidligere har fået injektionsbehandling mod allergi - det vides ikke, om IMULDOSA kan påvirke disse behandlinger.
- Hvis du er over 65 år - i så fald kan du være mere tilbøjelig til at få infektioner.
Tal med din læge eller apotekspersonalet, før du begynder at bruge IMULDOSA, hvis du ikke er sikker på, om noget af ovenstående gælder for dig.
Visse patienter har oplevet lupus-lignende reaktioner, herunder kutan lupus eller lupus-lignende syndrom, under behandlingen med ustekinumab. Tal straks med din læge, hvis du oplever et rødt, hævet, skællende udslæt, sommetider med en mørkere kant, i områder af huden, der er udsat for sollys, eller hvis du samtidig har ledsmerter.
Hjerteanfald og slagtilfælde
Hjerteanfald og slagtilfælde har været set i forsøg med patienter med psoriasis, som blev behandlet med ustekinumab. Din læge vil regelmæssigt kontrollere dine risikofaktorer for hjertesygdom og slagtilfælde for at sikre, at disse behandles på passende vis. Du skal øjeblikkeligt søge lægehjælp, hvis du oplever smerter i brystet, kraftesløshed eller en unormal fornemmelse i den ene side af kroppen, asymmetrisk ansigt eller tale- eller synsforstyrrelser.
Børn og unge
Det frarådes at give IMULDOSA til børn med psoriasis under 6 år, og til børn under 18 år med psoriasisartrit og Crohns sygdom, da det ikke er undersøgt hos denne aldersgruppe.
Brug af andre lægemidler eller vacciner sammen med IMULDOSA
Fortæl det altid til lægen eller apotekspersonalet:
- hvis du tager andre lægemidler, for nylig har taget andre lægemidler eller planlægger at tage andre lægemidler.
- hvis du er blevet vaccineret for nylig eller skal have en vaccination. Visse typer vaccine (levende vacciner) må ikke gives, mens du er i behandling med IMULDOSA.
- hvis du har fået IMULDOSA, mens du var gravid, skal du fortælle dit barns læge om din behandling med IMULDOSA, før barnet bliver vaccineret, herunder med levende vacciner som for eksempel BCG-vaccine (der bruges til at forebygge tuberkulose). Levende vacciner frarådes til dit barn i de første tolv måneder efter fødslen, hvis du har fået IMULDOSA, mens du var gravid, medmindre dit barns læge anbefaler andet.
Graviditet og amning
- Hvis du er gravid, har mistanke om, at du er gravid eller planlægger at blive gravid, skal du spørge din læge til råds, før du tager dette lægemiddel.
- Der er ikke set en øget risiko for fødselsdefekter hos børn, der har været udsat for Imuldosa i livmoderen. Der er dog begrænset erfaring med Imuldosa hos gravide kvinder. Det er derfor bedst at lade være med at bruge Imuldosa under graviditet.
- Hvis du er en kvinde i den fødedygtige alder, rådes du til at undgå at blive gravid, og du skal bruge sikker prævention, mens du bruger Imuldosa og i mindst 15 uger efter den sidste behandling med Imuldosa.
- Imuldosa kan blive overført til det ufødte barn via moderkagen. Hvis du har fået Imuldosa, mens du var gravid, kan dit barn have en højere risiko for at få en infektion.
- Hvis du har fået Imuldosa, mens du var gravid, er det vigtigt, at du fortæller det til dit barns læger og andet sundhedspersonale, før barnet bliver vaccineret. Hvis du har fået Imuldosa, mens du var gravid, frarådes det, at dit barn bliver vaccineret, herunder med levende vacciner som for eksempel BCG-vaccine (der bruges til at forebygge tuberkulose) i de første tolv måneder efter fødslen, medmindre dit barns læge anbefaler andet.
- Ustekinumab kan passere over i modermælken i meget små mængder. Tal med din læge, hvis du ammer eller planlægger at amme. Sammen med din læge skal du beslutte, om du skal amme eller bruge Imuldosa - du må ikke begge dele.
Trafik- og arbejdssikkerhed
IMULDOSA påvirker ikke eller kun i ubetydelig grad arbejdssikkerheden eller evnen til at færdes sikkert i trafikken.
IMULDOSA indeholder polysorbat 80
IMULDOSA indeholder 0,02 mg polysorbat 80 (E433) i hver dosisenhed, svarende til 0,04 mg/ml.
Polysorbater kan forårsage allergiske reaktioner. Fortæl det til din læge, hvis du har kendt allergi.
3. Sådan skal du bruge IMULDOSA
IMULDOSA er beregnet til brug under vejledning og tilsyn af en læge med erfaring i at behandle de sygdomme, som IMULDOSA er beregnet til.
Brug altid IMULDOSA nøjagtigt efter lægens anvisning. Er du i tvivl, så spørg lægen. Tal med lægen om, hvornår du skal have dine injektioner og opfølgende kontrol.
Hvor meget IMULDOSA skal du have
Lægen beslutter, hvor meget IMULDOSA du har brug for og i hvor lang tid.
Voksne på 18 år og derover
Psoriasis og/eller psoriasisartrit
- Den anbefalede startdosis er 45 mg IMULDOSA. Patienter, som vejer mere end 100 kg, kan starte med en dosis på 90 mg i stedet for 45 mg.
- Efter startdosen skal du have den næste dosis 4 uger senere og dernæst hver 12. uge. De efterfølgende doser er sædvanligvis de samme som startdosen.
Crohns sygdom
- Du vil få den første dosis på ca. 6 mg/kg IMULDOSA af din læge gennem et drop i en blodåre i armen (intravenøs infusion). Efter den indledende dosis skal du have den næste dosis på 90 mg IMULDOSA som en injektion under huden (subkutant) 8 uger senere og derefter hver 12. uge.
- Efter den første injektion under huden vil visse patienter muligvis få 90 mg IMULDOSA hver 8. uge. Din læge beslutter, hvornår du skal have din næste dosis.
Børn og unge på 6 år og derover
Psoriasis
- Lægen vil fastlægge den rigtige dosis til dig, herunder den mængde (det volumen) af IMULDOSA, der skal injiceres for at give den rigtige dosis. Den rigtige dosis til dig afhænger af din kropsvægt på det tidspunkt, hvor den enkelte dosis gives.
- Hvis du vejer mindre end 60 kg, er der ikke nogen doseringsform for IMULDOSA til børn under 60 kg kropsvægt og der skal derfor anvendes et andet ustekinumab-præparat.
- Hvis du vejer 60-100 kg, er den anbefalede dosis 0,45 mg IMULDOSA.
- Hvis du vejer over 100 kg, er den anbefalede dosis 90 mg IMULDOSA.
- Efter startdosen skal du have den næste dosis 4 uger senere og derefter hver 12. uge.
Sådan får du IMULDOSA
- IMULDOSA gives som indsprøjtning (injektion) under huden (subkutant). I begyndelsen af behandlingen kan IMULDOSA indsprøjtes (injiceres) af en læge eller sygeplejerske.
- Du og din læge kan beslutte, at du selv injicerer IMULDOSA. I så fald vil du få undervisning i, hvordan du skal gøre dette.
- Nærmere instruktioner i at give IMULDOSA finder du under "Vejledning i injektion" sidst i denne indlægsseddel.
Tal med din læge, hvis du har spørgsmål i forbindelse med at give dig selv en injektion.
Hvis du har brugt for meget IMULDOSA
Kontakt lægen, skadestuen eller apotekspersonalet, hvis du har brugt eller fået for meget IMULDOSA. Tag æsken med, selv hvis den er tom.
Hvis du har glemt at bruge IMULDOSA
Kontakt lægen eller apotekspersonalet, hvis du glemmer en dosis. Du må ikke tage en dobbeltdosis som erstatning for den glemte dosis.
Hvis du holder op med at bruge IMULDOSA
Det er ikke farligt at holde op med at bruge IMULDOSA. Hvis du stopper behandlingen, kan dine symptomer dog komme tilbage.
Spørg lægen eller apotekspersonalet, hvis der er noget, du er i tvivl om.
4. Bivirkninger
Dette lægemiddel kan som alle andre lægemidler give bivirkninger, men ikke alle får bivirkninger.
Alvorlige bivirkninger
Nogle patienter kan få alvorlige bivirkninger, der kan kræve omgående behandling.
Allergiske reaktioner - kan kræve omgående behandling. Kontakt straks lægen eller skadestue, hvis du bemærker nogle af følgende tegn:
- Alvorlige allergiske reaktioner (anafylaksi) er sjældne hos personer, der bruger IMULDOSA (kan forekomme hos op til 1 ud af 1.000 patienter). Tegnene omfatter:
- besvær med at trække vejret eller synke
- lavt blodtryk, som kan give svimmelhed eller omtågethed
- hævelser i ansigt, læber, mund eller svælg.
- Almindelige tegn på en allergisk reaktion omfatter hududslæt og nældefeber (kan forekomme hos op til 1 ud af 100 patienter).
I sjældne tilfælde er der blevet indberettet allergiske lungereaktioner og lungebetændelse hos patienter, der fik ustekinumab. Kontakt straks lægen, hvis du får symptomer som for eksempel hoste, åndenød og feber.
Hvis du får en alvorlig allergisk reaktion, vil lægen måske beslutte, at du ikke må få IMULDOSA igen.
Infektioner - kan kræve omgående behandling. Kontakt straks lægen, hvis du bemærker nogle af følgende tegn:
- Næse- og halsinfektioner og forkølelser er almindelige (kan forekomme hos op til 1 ud af 10 patienter)
- Brystinfektioner er ikke almindelige (kan forekomme hos op til 1 ud af 100 brugere)
- Betændelse i vævet under huden (cellulitis) er ikke almindelig (kan forekomme hos op til 1 ud af 100 patienter)
- Helvedesild (et smertefuldt udslæt med blærer) er ikke almindeligt (kan forekomme hos op til 1 ud af 100 patienter).
IMULDOSA kan nedsætte din evne til at bekæmpe infektioner. Nogle infektioner kan blive alvorlige og kan omfatte infektioner, der skyldes virusser, svampe, bakterier (herunder tuberkulose) eller parasitter, herunder infektioner, som hovedsagelig forekommer hos personer med svækket immunforsvar (opportunistiske infektioner). Der er rapporteret om opportunistiske infektioner i hjerne (encephalitis, meningitis), lunger og øjne hos patienter, der er blevet behandlet med ustekinumab.
Vær opmærksom på tegn på infektion, når du bruger IMULDOSA. De kan omfatte:
- feber, influenzalignende symptomer, nattesved, vægttab
- træthedsfølelse, kortåndethed, vedvarende hoste
- varm, rød eller smertefuld hud eller et smertefuldt udslæt med blærer
- svien ved vandladning
- diarré
- synsforstyrrelser eller synstab
- hovedpine, nakkestivhed, lysfølsomhed, kvalme eller forvirring.
Fortæl det straks til lægen, hvis du bemærker et af disse tegn på infektion. De kan være tegn på infektioner som brystinfektioner, hudinfektioner, helvedesild eller opportunistiske infektioner, som kan medføre alvorlige komplikationer. Fortæl det til lægen, hvis du får en infektion, der ikke vil gå væk eller bliver ved med at vende tilbage. Din læge kan beslutte, at du ikke må få IMULDOSA, før infektionen er væk. Fortæl også din læge, hvis du har åbne rifter eller sår, da der kan gå betændelse i dem.
Hudafskalning - øget rødme og afskalning af huden på et større område af kroppen kan være symptomer på sygdommene erytroderm psoriasis eller eksfoliativ dermatitis, som er alvorlige hudsygdomme. Kontakt straks lægen, hvis du bemærker et af disse tegn.
Andre bivirkninger
Almindelige bivirkninger (kan forekomme hos op til 1 ud af 10 patienter):
- Diarré
- Kvalme
- Opkastning
- Træthed
- Svimmelhed
- Hovedpine
- Kløe
- Ryg-, muskel- eller ledsmerter
- Ondt i halsen
- Rødme og smerter på injektionsstedet
- Bihulebetændelse
Ikke almindelige bivirkninger (kan forekomme hos op til 1 ud af 100 patienter):
- Infektion i tænderne
- Svampeinfektion i skeden
- Depression
- Tilstoppet næse
- Blødning, blå mærker, hård hud, hævelser og kløe på injektionsstedet
- Følelse af svaghed
- Hængende øjenlåg og slappe muskler i den ene side af ansigtet (ansigtslammelse eller Bells parese), sædvanligvis forbigående.
- Forandringer i psoriasis med rødme og nye bittesmå gule eller hvide blærer i huden, somme tider med feber (pustuløs psoriasis)
- Hudafskalning (hudeksfoliation)
- Acne
Sjældne bivirkninger (kan forekomme hos op til 1 ud af 1.000 patienter):
- Rødme og afskalning af huden på et større område af kroppen, som kan klø eller gøre ondt (eksfoliativ dermatitis). Somme tider udvikles der lignende symptomer som en naturlig ændring i symptomerne på psoriasis (erytroderm psoriasis).
- Betændelse i små blodkar, hvilket kan føre til et hududslæt med små røde eller lilla knopper, feber eller ledsmerter (vaskulitis).
Meget sjældne bivirkninger (kan forekomme hos op til 1 ud af 10.000 patienter):
- Blærer på huden, som kan være røde, kløende og smertefulde (bulløs pemphigoid).
- Kutan lupus eller lupus-lignende syndrom (rødt, hævet, skællende udslæt på områder af huden, der er udsat for sollys, eventuelt med samtidige ledsmerter).
Indberetning af bivirkninger
Hvis du oplever bivirkninger, bør du tale med din læge, apotekspersonalet eller sygeplejersken. Dette gælder også mulige bivirkninger, som ikke er medtaget i denne indlægsseddel. Du eller dine pårørende kan også indberette bivirkninger direkte til Lægemiddelstyrelsen
Lægemiddelstyrelsen
Axel Heides Gade 1
DK-2300 København S
Websted: www.meldenbivirkning.dk
Ved at indrapportere bivirkninger kan du hjælpe med at fremskaffe mere information om sikkerheden af dette lægemiddel.
5. Opbevaring
- Opbevar lægemidlet utilgængeligt for børn.
- Opbevares i køleskab (2 °C - 8 °C). Må ikke nedfryses.
- Opbevar den fyldte injektionssprøjte i den ydre karton for at beskytte det mod lys.
- Hvis det er nødvendigt, kan den enkelte fyldte IMULDOSA-injektionssprøjte også opbevares ved stuetemperatur op til 30 °C i en enkelt periode på maksimalt 30 dage i den oprindelige karton for at beskytte mod lys. Anfør den dato, hvor den fyldte sprøjte tages ud af køleskabet første gang, og den dato, hvor den skal kasseres, i felterne på yderkartonen. Datoen, hvor sprøjten skal kasseres, må ikke være senere end den oprindelige udløbsdato, der er trykt på kartonen. Når en sprøjte har været opbevaret ved stuetemperatur (op til 30 °C), må den ikke anbringes i køleskabet igen. Kassér sprøjten, hvis den ikke bruges inden for 30 dage ved opbevaring ved stuetemperatur, eller hvis den oprindelige udløbsdato er nået, afhængigt af hvilken dato, der kommer først.
- Ryst ikke den fyldte IMULDOSA-injektionssprøjte. Langvarig, voldsom rysten kan ødelægge lægemidlet.
Brug ikke IMULDOSA
- efter den udløbsdato, der står på etiketten og æsken efter "EXP". Udløbsdatoen er den sidste dag i den nævnte måned.
- hvis væsken er misfarvet, uklar, eller der flyder fremmedlegemer i den (se afsnit 6 "Udseende og pakningsstørrelser").
- hvis du ved eller tror, at IMULDOSA er blevet udsat for ekstreme temperaturer ved en fejltagelse (f.eks. frost eller varme).
- hvis produktet er blevet rystet voldsomt.
IMULDOSA er kun til engangsbrug. Eventuelt ikke anvendt lægemiddel, der er tilbage i injektionssprøjten, skal bortskaffes. Spørg apotekspersonalet, hvordan du skal bortskaffe lægemiddelrester. Af hensyn til miljøet må du ikke smide lægemiddelrester i afløbet, toilettet eller skraldespanden.
6. Pakningsstørrelser og yderligere oplysninger
IMULDOSA indeholder:
- Aktivt stof: Ustekinumab. Hver fyldt injektionssprøjte indeholder 45 mg ustekinumab i 0,5 ml.
- Øvrige indholdsstoffer: L-histidin, L-histidin-hydrochlorid-monohydrat, polysorbat 80 (E433), saccharose og vand til injektionsvæsker.
Udseende og pakningsstørrelser
IMULDOSA er en farveløs til lys gul og klar til let opaliserende opløsning. Den udleveres i en karton, der indeholder 1 dosis i en 1 ml-injektionssprøjte af glas. Hver injektionssprøjte indeholder 45 mg ustekinumab i 0,5 ml injektionsvæske.
Indehaver af markedsføringstilladelsen og fremstiller
Indehaver af markedsføringstilladelsen
Accord Healthcare S.L.U.
World Trade Center, Moll de Barcelona, s/n
Edifici Est, 6a Planta
08039 Barcelona
Spanien
Fremstiller
Accord Healthcare Polska Sp. z.o.o.
ul. Lutomierska 50,
95-200, Pabianice
Polen
Accord Healthcare B.V.
Winthontlaan 200,
3526 KV Utrecht
Holland
Hvis du ønsker yderligere oplysninger om dette lægemiddel, skal du henvende dig til den lokale repræsentant for indehaveren af markedsføringstilladelsen:
AT / BE / BG / CY / CZ / DE / DK / EE / ES / FI / FR / HR / HU / IE / IS / IT / LT / LV / LU / MT / NL / NO / PL / PT / RO / SE / SI / SK
Accord Healthcare S.L.U.
Tlf: +34 93 301 00 64
EL
Win Medica Α.Ε.
Τηλ: +30 210 74 88 821
Du kan finde yderligere oplysninger om dette lægemiddel på Det Europæiske Lægemiddelagenturs hjemmeside: https://www.ema.europa.eu.
Brugervejledning
Vejledning i injektion
Når behandlingen påbegyndes, vil din læge eller sygeplejerske hjælpe dig med den første injektion (indsprøjtning). Men du og din læge kan beslutte, at du selv injicerer (indsprøjter) IMULDOSA. Hvis dette er tilfældet, vil du få undervisning i, hvordan du injicerer IMULDOSA. Tal med din læge, hvis du har spørgsmål i forbindelse med at give dig selv en injektion.
- Bland ikke IMULDOSA med andre væsker til injektion
- Ryst ikke de fyldte injektionssprøjter med IMULDOSA. Voldsom rysten kan ødelægge lægemidlet. Brug ikke lægemidlet, hvis det er blevet rystet voldsomt.
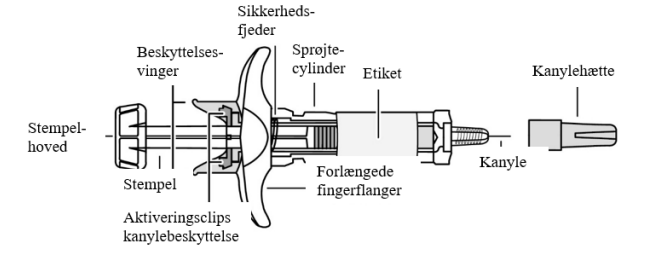
Figur 1 viser, hvordan en fyldt injektionssprøjte ser ud.
Figur 1
1. Kontrollér antallet af fyldte injektionssprøjter og forbered udstyret:
Forberedelse til anvendelse af den fyldte injektionssprøjte
- Tag de(n) fyldte injektionssprøjte(r) ud af køleskabet. Lad den fyldte injektionssprøjte stå uden for kartonen i ca. en halv time. Derved får væsken en passende temperatur til injektion (stuetemperatur). Fjern ikke injektionssprøjtens kanylehætte, mens væsken får lov til at få stuetemperatur.
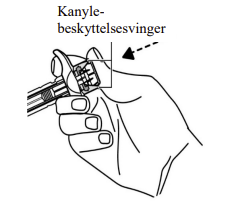
- Hold om den fyldte injektionssprøjte omkring cylinderen med den beskyttede kanyle opad.
- Hold ikke om stempelhovedet, stemplet, beskyttelsesvingerne eller kanylehætten.
- Træk ikke tilbage i stemplet på noget tidspunkt.
- Fjern ikke kanylehætten fra den fyldte injektionssprøjte, før du bliver instrueret om det.
- Rør ikke aktiveringsclipsene til kanylebeskyttelse for at undgå for tidlig tildækning af kanylen med kanylebeskyttelsen.
Kontrollér de(n) fyldte injektionssprøjte(r) for at sikre
- at antallet af fyldte injektionssprøjter og styrken er korrekt
- Hvis din dosis er 45 mg, får du en fyldt injektionssprøjte med 45 mg IMULDOSA.
- Hvis din dosis er 90 mg, får du to fyldte injektionssprøjter med 45 mg IMULDOSA, og du skal give dig selv to injektioner. Vælg to forskellige steder til disse injektioner (f.eks. en injektion i det højre lår og den anden injektion i det venstre lår) og tag de to injektioner lige efter hinanden.
- at det er det rigtige lægemiddel
- at det ikke har overskredet udløbsdatoen
- at den fyldte injektionssprøjte ikke er beskadiget
- at opløsningen i den fyldte injektionssprøjte er farveløs til let gul og klar til svagt opaliserende
- at opløsningen i den fyldte injektionssprøjte ikke er misfarvet eller uklar og at den ikke indeholder fremmede partikler
- at opløsningen i den fyldte injektionssprøjte ikke er frossen.
Find alt det frem, som du har brug for, og læg det ud på en ren overflade. Det omfatter desinficerende servietter, en vattot eller et stykke gaze og en affaldsbeholder til skarpe genstande.
2. Vælg og forbered injektionsstedet:
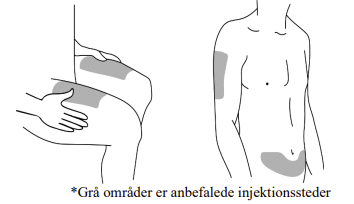
Vælg et injektionssted (se figur 2).
- IMULDOSA gives som injektion under huden (subkutant).
- Gode steder til injektionen er øverste del af låret eller omkring maven (abdomen) mindst 5 cm fra navlen.
- Hvis det er muligt, skal du undgå at bruge hudområder med tegn på psoriasis.
- Hvis der er en, der vil hjælpe med at give dig injektionen, kan han eller hun også vælge overarmene som injektionssted.
Figur 2
Forbered injektionsstedet
- Vask dine hænder grundigt med sæbe og varmt vand.
- Tør injektionsstedet af med en desinficerende serviet.
- Rør ikke dette område igen, før du har givet injektionen.
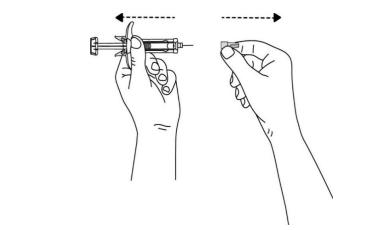
3. Fjern kanylehætten (se figur 3).
- Kanylehætten må ikke fjernes, før du er klar til at injicere dosis.
- Tag den fyldte injektionssprøjte op. Hold om injektionssprøjtens cylinder med én hånd.
- Træk kanylehætten lige af og smid den væk. Rør ikke ved stemplet, mens du gør dette.
Figur 3
- Du vil måske bemærke en luftboble i den fyldte injektionssprøjte eller en dråbe væske ved spidsen af kanylen. Begge dele er normalt, og de behøver ikke fjernes.
- Rør ikke kanylen, og lad den ikke berøre nogen overflade.
- Brug ikke den fyldte injektionssprøjte, hvis den tabes, uden at kanylehætten er sat på. Hvis dette sker, så kontakt din læge eller apotekspersonalet.
- Foretag injektionen straks efter at have fjernet kanylehætten.
4. Indsprøjt dosis:
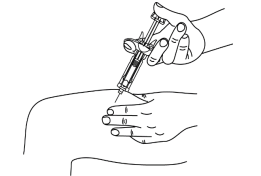
- Hold den fyldte injektionssprøjte mellem langfingeren og pegefingeren på den ene hånd, og placér tommelfingeren på toppen af stempelhovedet. Brug den anden hånd til forsigtigt at klemme den rengjorte hud mellem tommel- og pegefinger. Du må ikke klemme hårdt.
- Træk ikke tilbage i stemplet på noget tidspunkt.
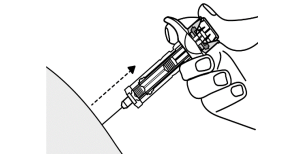
- Tryk kanylen igennem huden så langt, som den kan, med en enkelt, hurtig bevægelse (se figur 4).
Figur 4
- Indsprøjt alt lægemidlet ved at trykke stemplet ind, indtil stempelhovedet er helt nede mellem kanylebeskyttelsesvingerne (se figur 5).
Figur 5
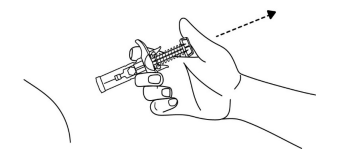
- Når stemplet er trykket så langt ind, som det kan, fortsæt da med at holde trykket på stempelhovedet, træk kanylen ud og slip huden (se figur 6).
Figur 6
- Fjern langsomt tommelfingeren fra stempelhovedet, og lad den tomme injektionssprøjte bevæge sig op, indtil hele kanylen er dækket af kanylebeskyttelsesvingerne, som vist på figur 7.
Figur 7
5. Efter indsprøjtningen:
- Tryk en desinficerende serviet på injektionsstedet i et par sekunder efter injektionen.
- Der kan være en lille smule blod eller væske på injektionsstedet. Det er normalt.
- Du kan presse en vattot eller et stykke gaze på injektionsstedet og holde det der i 10 sekunder.
- Gnid ikke huden på injektionsstedet. Du kan dække injektionsstedet med et lille plaster, hvis det er nødvendigt.
6. Bortskaffelse
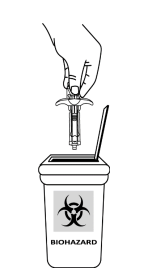
- Brugte injektionssprøjter skal anbringes i en punktérfri beholder beregnet til skarpe ting (se figur 8). Genbrug aldrig en injektionssprøjte for din sikkerheds og dit helbreds skyld og af hensyn til andres sikkerhed. Beholderen med brugte injektionssprøjter bortskaffes i henhold til lokale retningslinjer.
Figur 8
Revisionsdato
Denne indlægsseddel blev senest ændret 06/2025